CUSTOMER CENTER
CIRS는 기업이 만들어내는 안전한 제품 개발을 돕는 인증 · 검사 서비스를 제공하고 있습니다.
CIRS는 기업이 만들어내는 안전한 제품 개발을 돕는 인증 · 검사 서비스를 제공하고 있습니다.
# 3월 5일, 유럽소비자안전과학위원회(이하 SCCS)가 향료 성분 아세틸레이티드 베티버 오일 Acetylated Vetiver Oil(AVO)(CAS No 84082-84-8, EC No 282-031-1)의 스프레이 화장품 내 흡입 독성에 대한 예비 의견(SCCS/1663/24) 발표 (공개 의견 요청 마감일은 2024년 5월 3일)
제공된 흡입 독성 데이터를 기반으로 SCCS는 스프레이 화장품에 아세틸레이티드 베티버 오일(AVO)을 사용하는 것이 안전하다고 생각하나? SCCS는 제공된 흡입독성과 총노출량 관련 데이터를 고려해 방향형 스프레이에서는 0.9%(w/w), 탈취제 스프레이에서는 0.05%(w/w), 헤어젤 스프레이 및 바디로션 스프레이에서는 0.1%(w/w)의 예상 최대 농도로 아세틸레이티드 베티버 오일(1% 알파-토코페롤 함유)을 사용하는 것이 안전하다고 판단했습니다.
# 3월 5일, SCCS가 하이드록시프로필 p-페닐렌디아민(CAS No. 73793-79-0/EC No. 827-723-1)과 그 디하이드로클로라이드염(CAS No. 1928659-47-5/) 관련 최종 의견(SCCS/1659/23) 발표
제시된 데이터에 따라 SCCS는 산화형 염색 제품에 최대 농도 2%의 하이드록시프로필 p-페닐렌디아민과 그 디하이드로클로라이드 염을 사용하는 것이 안전하다고 간주합니다. 시험물질이 경증에서 중간 정도의 눈 자극을 유발할 가능성은 배제할 수 없습니다. 동물 실험 데이터에 따르면 하이드록시프로필 p-페닐렌디아민과 그 디하이드로클로라이드 염은 중간 정도의 피부 알레르기 물질입니다.
# 3월 11일, SCCS가 헥실살리실레이트(Hexyl Salicylate, CAS/EC No. 6259-76-3/228-408-6) 관련 최종 의견(SCCS/1658/23) 발표
(1) 제공된 데이터와 잠재적인 내분비 교란 특성과 관련된 문제를 고려하여 SCCS는 본 의견의 표 1에 제시된 최대 농도에서 헥실 살리실레이트를 사용하는 것은 안전하다고 간주합니다.
표 1: 제출 문서 중 화장품 내 헥실살리실레이트의 최대 사용 농도
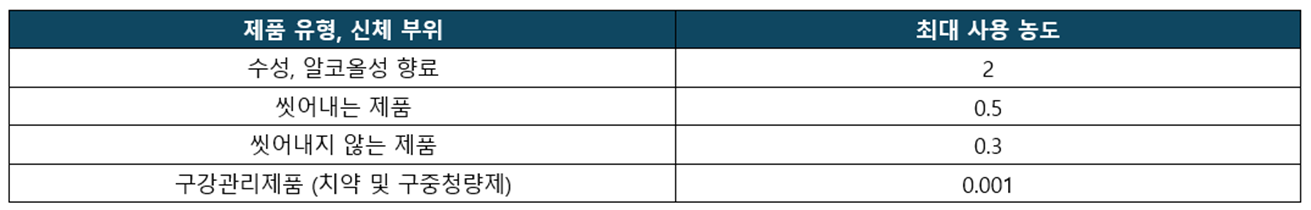
(2) 신청자는 어린이 사용 화장품의 구체적인 시나리오(피부 접촉 노출)는 제공하지 않았으며 특정 노출 매개변수(체중, 제품 사용량, 신체 표면적 등)의 연령별 차이도 고려하지 않았습니다. 그러나 SCCS는 성인의 안전역(MoS)이 100보다 훨씬 높은 것에 비추어 이 연령대의 어린이가 사용하는 제품 범주를 고려하면 3~10세 어린이의 안전역도 100보다 높을 것이라는데 주목했습니다. 또한 SCCS의 임무는 환경 측면을 포함하지 않습니다. 따라서 이 평가는 헥실살리실레이트의 환경에 대한 안전성을 다루지 않습니다.
# 3월 12일, 영국 보건안전집행국(HSE) 25개 화학 물질을 영국 의무 분류 라벨링 목록(MCL)에 추가
여기에는 화장품 원료 용도 성분인 2-에틸헥산산(Ethylhexanoic acid) 및 그 염류(CMR 물질로 분류, 생식 독성 1B), 디메틸아미노톨루엔(CMR 물질로 분류, 발암성 1B)이 포함됩니다. 영국은 이 두 원료를 영국 화장품 법규 부속서 II에 추가하고 화장품에 사용하는 것을 금지합니다.
# 3월 14일, 유럽 위원회는 EU 화장품 규정(EC) 1223/2009를 개정하고 EU 화장품 규정(EC) No 1223/2009 내의 화장품 금지 물질 목록(부속서 II) 및 제한 물질 목록(부속서 III)을 개정하는 규정(EU) 2024/858을 발표했으며, 이 중 부속서 II에 여러가지 나노 물질이 신규로 추가되고 부속서 III에 새로운 하이드록시아파타이트(나노)의 사용 제한 추가
화장품 사용금지 물질 목록(부속서 Ⅱ)에 다음 12가지 물질을 포함시킬 것을 통보
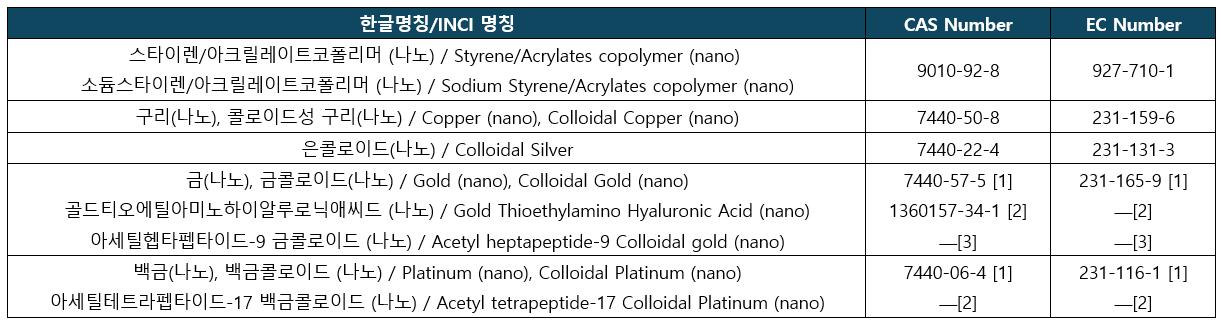
2025년 2월 1일부터 이 물질을 함유한 화장품은 EU 시장에 출시할 수 없습니다. 2025년 11월 1일부터 이 물질을 함유한 화장품을 EU 시장에서 판매할 수 없습니다.
하이드록시아파타이트(나노)을 화장품 제한물질 목록에 포함시킬 것을 통보(부속서 Ⅲ)
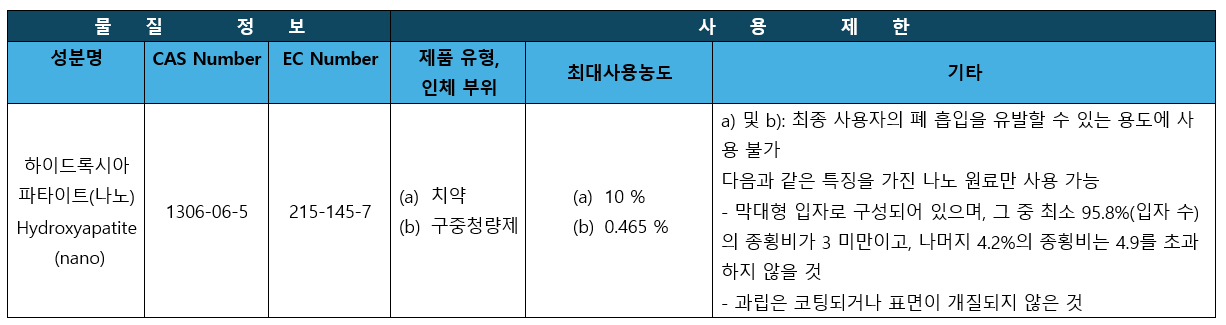
2025년 2월 1일부터 이 물질을 함유하고 제한 규정을 충족하지 않는 화장품은 EU 시장에 진입할 수 없습니다. 2025년 11월 1일부터 이 물질을 함유한 화장품을 EU 시장에서 판매할 수 없습니다.
# 4월 3일, 유럽 위원회는 법규(EU) 2024/996을 발표하고, (EC) 1223/2009 유럽 연합 화장품 규정을 개정
4-메칠벤질리덴캠퍼(4-Methylbenzylidene Camphor, 4-MBC) 사용 금지
2025년 5월 1일부터 이 물질을 함유한 화장품은 유럽 시장에 출시할 수 없습니다. 2026년 5월 1일부터 이 물질을 함유한 화장품은 유럽 시장에서 판매될 수 없습니다.
--> CIRS 의견: 우리나라에서는 4% 한도로 사용이 허용되는 자외선 차단제 성분이므로 2025년5월부터 유럽 수출 시에는 성분 변경이 필요합니다.
여러가지 제한 성분 신규 추가
== 신규 추가 성분: 알파알부틴(Alpha-Arbutin*), 알부틴(Arbutin*), 제니스테인(Genistein*), 다이드제인(Daidzein*), 코직애씨드(Kojic Acid*), 레티놀(Retinol**), 레티닐아세테이트(Retinyl Acetate*), 레티닐팔미테이트(Retinyl Palmitate**) 등의 제한 성분
(*) 2025년 2월 1일부터 이 물질을 함유하면서 조건을 충족하지 않는 화장품은 유럽 시장에 출시할 수 없습니다. 2025년 11월 1일부터 이 물질을 함유하면서 조건을 충족하지 않는 화장품은 유럽 시장에서 판매될 수 없습니다.
(**) 2025년 11월 1일부터 이 물질을 함유하면서 요건을 충족하지 않는 화장품은 유럽시장에 출시할 수 없습니다. 2027년 5월 1일부터 이 물질을 함유하면서 조건을 충족하지 않는 화장품은 유럽 시장에서 판매될 수 없습니다.
트리클로카반(Triclocarban)과 트리클로산(Triclosan)의 사용 요구 사항 수정
이 물질을 함유하고 있지만 조건을 충족하지 않는 화장품은 2024년 4월 23일에 적용되는 조건을 충족하면 2024년 12월 31일 이전에 유럽 시장에 출시될 수 있으며, 해당 날짜 이전에 출시되면 2025년 10월 31일 이전에는 유럽 시장에서 계속 판매될 수 있습니다.
원래의 4-메칠벤질리덴캠퍼(4-Methylbenzylidene Camphor) 사용 요구 사항 삭제
부속서 VI(화장품 준용 자외선 차단제 목록)에서 제18조(원래의 4-메칠벤질리덴캠퍼 사용 요건)를 삭제하며 2025년 5월 1일부터 적용됩니다.
# 4월 4일, SCCS가 벤조페논-4(Benzophenone-4, CAS No. 4065-45-6, EC No. 223-772-2) 관련 최종안전의견(SCCS/1660/23) 발표
안전성 평가에 근거하고 벤조페논-4의 잠재적인 내분비 교란 특성으로 인한 우려를 고려하여 SCCS는 벤조페논-4가 자외선 필터로서 자외선 차단제, 크림 및 핸드크림, 립스틱, 자외선 차단 스프레이 및 펌프형 스프레이의 사용 농도가 최대 5%에 달하며 단독 또는 혼합 사용 여부에 상관없이(확정성에 기반한 종합 노출 평가) 모두 안전하다고 간주합니다. 예를 들어 빛에 노출된 화장품 제형의 안정제로서 아세톤-4를 추가로 사용하는 어떠한 경우라도 자외선 필터로서의 용도를 포함하여 위에서 언급한 농도 범위(즉, 5%) 내에서 유지되어야 합니다.
# 4월 12일 뉴질랜드 화장품에 PFAS 사용을 금지, 2026년 12월 31일부터 시행
최근 뉴질랜드 환경보호청은 소비자와 환경을 보호하기 위해 화장품에 과불화화합물(PFAS)의 사용을 금지하는 획기적인 조치를 취했습니다. 이 금지령을 시행하여 뉴질랜드는 이러한 지속적인 '영구적 화학 물질'에 대한 조치를 취한 세계 최초의 국가 중 하나가 되었습니다.
# 3월 21일, 대만 <화장품 사용 금지 성분표> 개정, 엑소좀 검사 송부 문서를 발표
대만은 'Cells, tissues or products of human origin'(인간 유래 세포, 조직 또는 제품) 및 'Zirconium and its compounds'(지르코늄 및 그 화합물) 등 2개 성분 정보 명칭을 개정하고 '아미노카프로산 및 그 염류' 등 9개 사용 금지 성분을 추가했습니다. '인간 세포, 조직 또는 제품'에 대한 성분 개정 규정은 개정일부터 발효되었으며 나머지 개정은 2025년 1월 1일부터 발효됩니다. 같은 날 <인체세포 유래 엑소좀을 화장품에 사용하는 신청시 심사를 위해 제출해야 하는 문건>이 발표되어 해당 일자로 효력이 발생되었습니다.