CUSTOMER CENTER
CIRS는 기업이 만들어내는 안전한 제품 개발을 돕는 인증 · 검사 서비스를 제공하고 있습니다.
CIRS는 기업이 만들어내는 안전한 제품 개발을 돕는 인증 · 검사 서비스를 제공하고 있습니다.
2024년3월29일 중국식품약품검정원(NIFDC)은 <화장품안전성평가자료 제출지침(의견수렴고)>에 대한 공개 의견 수렴 관련 통지를 발표했습니다.

<화장품 안전성평가자료 제출지침(의견수렴고)》에서는 리스크 관리 원칙에 근거하여 화장품 안전성평가자료 제출 상황을 분류하며, 또한 화장품 안전성평가 보고서에 대한 자체 점검 요약서를 작성하고 기업이 제품 안전 평가 작업을 수행하도록 안내합니다.
1. 화장품 유형
<화장품 분류규칙 및 분류목록>의 분류규칙에 근거하여 화장품 효능 클레임, 작용 부위, 제품 제형, 사용 대상의 다양한 차원의 분류를 기반으로 다양한 유형의 제품 리스크를 종합적으로 고려하고, 모니터링 기간에 속한 신원료 또는 나노 원료의 사용 여부, 기기 또는 도구와 함께 사용해야 하는지 여부, pH 범위 및 등의 분류 항목을 추가하고 리스크 정도에 따라 화장품을 3개 유형으로 나눕니다.
(1) 제1유형 화장품
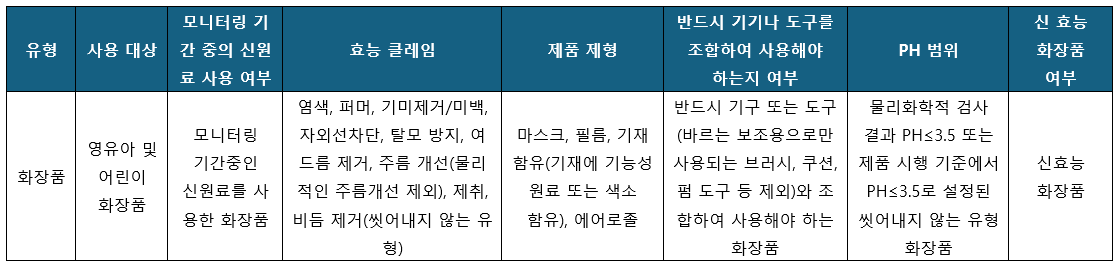
*제1유형 화장품의 경우 화장품 안정성 평가 자료를 제출해야 합니다.
(2) 제2유형 화장품
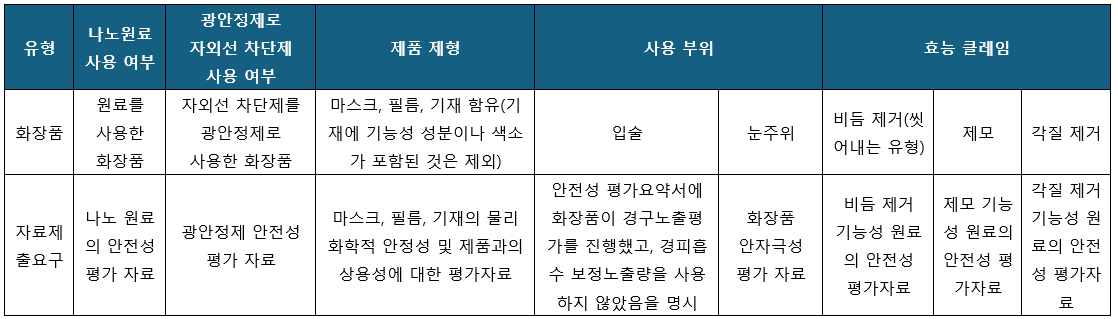
*관련 평가 자료의 요구 사항을 충족한다는 전제 하에 화장품 안전성 평가 결론만 제출하고 향후 참조를 위해 안전성 평가 보고서를 보관할 수 있습니다.
(3) 제3유형 화장품
제1유형 및 제2유형을 제외한 기타 일반 화장품으로 안전성 평가 결론만 제출하면 되고, 향후 참조를 위해 안전성 평가 보고서를 보관할 수 있습니다.
또한, 제2유형 및 제3유형 화장품의 경우, 출시 후 감독에서 생산 중단, 수입 및 판매와 같은 문제가 발생할 경우 영업일 기준 30일 이내에 화장품 안전성평가 보고서를 추가로 제출해야 합니다.
# 기타 안전성평가보고서를 제출하는 경우
화장품 등록인이 <화장품감독관리조례> 제59조, 제60조를 위반하여 법에 따라 행정처벌을 받은 경우, 행정처벌 결정일로부터 1년 이내에 등록을 진행한 화장품은 안전성평가 보고서를 제출해야 합니다.
<화장품감독관리조례> 제59조에 규정된 상황은 다음과 같습니다.
(1) 허가를 거치지 않고 화장품 생산활동에 종사한 경우, 또는 화장품허가인, 등록인이 화장품생산허가를 취득하지 않은 기업에게 화장품생산을 의뢰하 경우
(2) 허가증을 받지 않은 특수 화장품을 생산 또는 수입한 경우
(3) 화장품 생산에 사용을 금지하는 원료를 사용했거나 응당 허가를 받아야 하지만 허가를 받지 않은 신원료를 사용하여 화장품을 생산하였거나, 화장품에 인체 건강에 해를 끼칠 가능성이 있는 물질을 불법으로 첨가하였거나 사용기한이 지났거나, 폐기 또는 회수한 화장품 또는 원료로 화장품을 생산한 경우
<화장품감독관리조례> 제60조에 규정된 상황은 다음과 같습니다.
(1) 강제성 국가표준, 기술규범에 부합하지 않은 원료나 화장품과 직접적으로 접촉하는 포장재료를 사용하였거나, 응당 등록해야 하지만 등록하지 않은 화장품 신원료를 사용하여 화장품을 생산했거나, 강제성 국가표준 또는 기술규범의 요구에 따라 원료를 사용하지 않은 경우
(2) 강제성 국가표준, 기술규범의 요구에 부합하지 않거나 화장품 허가,등록자료에 명시한 기술요구에 부합하지 않은 화장품을 생산, 경영한 경우
(3) 화장품 생산품질 관리규범의 요구에 따라 생산하지 않은 경우
(4) 화장품의 사용기한을 변경한 경우
(5) 화장품 경영자가 임의로 화장품을 조제하였거나 변질, 사용기간이 지난 화장품을 경영한 경우
(6) 약품감독관리부문에서 회수를 명했지만 명령을 거부하고 회수하지 않았거나, 약품감독관리부문에서 생산, 경영을 일시 정지 또는 정지할 것을 명했지만 생산, 경영을 일시 정지 또는 정지하지 않은 경우
# 화장품 안전성 평가 보고서 자체 점검 요약서
화장품 원료의 안전성 평가는 다음의 증거 유형을 채택할 수 있습니다.
앞서 국가식품약품감독관리국의 <화장품 안전성평가 기술지침(2021년판)> 공고(2021년 제51호)를 발표하여 2024년 5월 1일 이후 화장품 허가인/등록인은 간소화된 제품 안전성평가 보고서를 종료하고, 제품 안전성 평가 보고서 전체 버전을 시작한다고 규정했습니다.
양자의 가장 큰 차이는 완전판 안전 평가 보고서가 더 이상 <기사용 화장품 원료 목록(2021년판)>의 최고 역사 사용량을 안전성 평가 증거로 사용하며 않으며, 해당 업체의 원료 역사 사용량(최소 3년)과 사용방법이 동일한 제품 내 농도도 더 이상 평가 증거로 채택하지 않는다는 점입니다.
그러나 이번 <제출 지침(의견 수렴고)>에서는 화장품 안전성평가 보고서 자체 점검 요약서에는 업체의 3년 원료 안전 역사 사용량을 평가 증거로 유지하고 있습니다.
이것은 3년 이상의 원료 역사를 가진 기업의 입장에서는 매우 유리한 조치로 업체가 안전성 평가 전체 버전의 과도기를 안정적이고 질서있게 지나갈 수 있게 해 줍니다.
위의 증거 중 임의의 하나를 사용할 수 없는 원료의 경우, <화장품 안전성 평가 기술 지침>의 리스크 평가 절차에 따라 원료의 위해성 식별 및 용량-반응 관계 평가를 수행해야 합니다.
노출 평가 및 리스크 특성 설명은 원료의 독성 평가 데이터, 평가 프로세스, 결과 및 결론 또는 제품 독성 테스트 데이터를 통해 제품 안전성을 증명합니다.
<자체점검 요약서>에서는 향정, 향료, 나노원료, 염색 제품의 착색제, 처방에 기재하지 않은 성분, 아직 안전모니터링 중인 신원료 등 중점적으로 주목하는 원료, 그리고 추진제를 함유한 스프레이 제품, 2제 또는 2제 이상 반드시 조합하여 사용해야 하는 제품, 기기 또는 도구와 병용해야 하는 제품, 어린이 화장품 등의 제품 안전성평가 기술 요약서에 대한 기술 지침을 제공합니다.
# 해석
이전에 NMPA의 <화장품 안전성평가 기술지침(2021년 판)> 공고(2021년 제51호) 발표에서는 2024년5월1일 이전에 화장품 허가인등록인은 "기술 지침"의 관련 요구사항에 따라 간소화 버전의 제품 안전성 평가보고서를 제출할 수 있다고 명시했습니다. 법규 규정에 따르면 현재 과도기에는 안전성 평가 보고서 간소화 버전이 사용되며, 올해 5월부터 기업은 안전성평가 보고서 전체 버전을 제공해야 합니다.